Tablica z charakterystycznymi danymi
Liczba elektronów: 13
Liczba neutronów: 14
Liczba protonów: 13
Elektroujemność (Allred-Rochow, Pauling): 1.47, 1.61
Stopień utlenienia: +3
Przewodność elektryczna: 369*105 1/(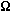 *m)
*m)
Gęstość (293 K): 2.702 g/cm3
Temperatura topnienia: 660,25°C, 933,25 K
Temperatura wrzenia: 2467°C, 2740 K
Molowa pojemność cieplna: 24.35 /(mol*K)
Ciepło topnienia: 10,79 kJ/mol
Ciepło parowania: 293,4 kJ/mol
Przewodność cieplna: 237 W/(m*K)
